Этот химический элемент известен человеку давно и сегодня используется буквально повсеместно. Электрические провода, посуда, монеты, строительные материалы – в наши дни медь и сплавы на её основе применяются в самых разных отраслях промышленности. Начало применения Cu относят к «Бронзовому веку» (3 тыс. лет до н.э.). Уже тогда люди умели добывать этот розово-золотистый металл и даже получать медно-оловяные сплавы. Вместе с тем, нахождение в природе меди совсем невелико: если изучить состав земной коры нашей планеты, то элемента Cu в неё окажется всего около 0,01% (23 место).
Медь: нахождение в природе

В природе медь встречается как в чистом виде (самородки могут достигать общего веса в несколько сотен тонн), так и в составе различных соединений. Обычно приходится иметь дело с сульфидами, сформировавшимися в осадочных горных породах, либо с субстратами. Получить медь из этих соединений легко благодаря низкой температуре плавления, чем и пользовались наши предки при изготовлении самых разных медных изделий.
Что касается названия элемента – Cuprum, то историки соотносят его с наименованием некогда древнегреческого острова Кипр (Cyprus), когда-то являвшегося наиболее крупным в Европе центром выработки материала. Вполне возможно впервые выплавлять медь научились именно на Кипре.
Физические свойства меди
Прежде всего, медь очень пластична, а потому крайне удобна в использовании, в частности, в плавке. Отличает этот металл и такая характеристика, как ярко выраженная окраска, которая делает материал декоративным (+ отжиг меди). Если для большинства известных металлов характерен серебристо-серый цвет, то Cu, наравне с золотом и осмием входит в число трёх с уникальной цветовой окраской.

Еще одно достоинство меди – высокая электропроводность, которая предопределяет использование данного металла в составе самой разной электропроводниковой продукции. Здесь же стоит сказать и о таком свойстве Cu, как отсутствие искры при ударе. Эта уникальная особенность меди делает её отличным материалом для изготовления деталей, работающих в условиях повышенной пожароопасности.
Химические свойства соединений меди
Особого внимания заслуживает взаимодействие Cu с кислотами. Так, этот элемент никак не реагирует на воду, растворы щелочей, соляную или разбавленную серную кислоты. При этом сильные окислители, такие как концентрированная серная или азотная кислота, очень быстро медь растворяют. Cu также называют коррозийностойким металлом, однако влажная атмосфера и углекислые газы, взаимодействуя с медью, способствуют образованию на её поверхности зеленоватого налета (карбонат меди).
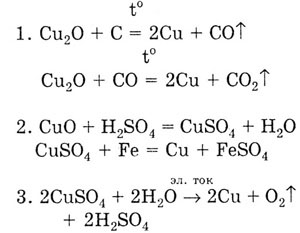
Сегодня широкое применение находят оксид (СuО), гидроксид (Си(ОН)2) и сульфид меди (CuS). Уникальное свойство сульфида меди – высокая электропроводность, позволяющая получать сверхпроводники. Химические свойства гидроксида меди позволяют легко получать оксиды (путем разложения гидроксида меди 2 при нагревании).
